A járvány korai szakaszában a gyors fejlődés miatt a gyanús betegek gyors diagnosztizálása a kulcsa a COVID-19 megelőzésének.Egyes jóváhagyott nukleinsav-detektáló reagensek fejlesztési ideje rövid, és olyan problémák lépnek fel, mint például a teljesítmény elsietett megerősítése, a reagensek nem megfelelő optimalizálása és a tételek közötti nagy különbségek;A különböző klinikai laboratóriumok problémái a nukleinsav-detektálási folyamat különböző aspektusaiban szintén befolyásolhatják a nukleinsav-detektálási eredmények pontosságát.Ez a cikk a jelenlegi SARS-CoV-2 nukleinsav-detektálás kulcsfontosságú kapcsolataira és pontjaira összpontosít, valamint elemzi a laboratóriumi nukleinsav-detektálás álnegatív és pozitív újravizsgálatának problémáit, valamint a klinikai inkonzisztenciát.
A SARS-CoV-2 nukleinsav kimutatásának elvei
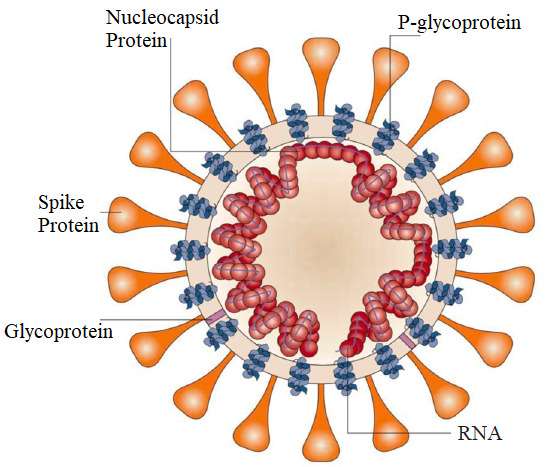
A SARS-CoV-2 egy körülbelül 29 kb méretű genomszekvenciájú, 10 gént tartalmazó RNS-vírus, amely 10 fehérjét képes hatékonyan kódolni.A vírusok RNS-ből és fehérjéből állnak, a legkülső réteg pedig lipidekből és glikoproteinekből álló külső bevonat.Belül a fehérjekapszid beburkolja az RNS-t, ezáltal védi a könnyen lebomló RNS-t (P1).
P1 A SARS-COV-2 felépítése
A vírusok specifikus sejtfelszíni receptorokon keresztül támadják meg a sejteket, hogy fertőzést okozzanak, és a gazdasejteket használják fel a replikációhoz.
A vírusos nukleinsav kimutatásának elve az, hogy a vírus RNS-t sejtlizátumon keresztül exponáljuk, majd valós idejű fluoreszcens reverz transzkripciós-polimeráz láncreakciót (RT-PCR) használunk a kimutatáshoz.
A kimutatási elv kulcsa a primerek és próbák használata a nukleinsavszekvenciák „célzott illeszkedésének” elérése érdekében, azaz a SARS-CoV-2 nukleinsavszekvenciájának megtalálása, amely körülbelül 30 000 bázisban különbözik a többi vírustól (a nukleinsav hasonlósága más vírusokhoz), „alacsony” terület, primerek és próbák tervezése.
A primerek és próbák nagymértékben illeszkednek a SARS-CoV-2 nukleinsav specifikus régiójához, vagyis a specificitás nagyon erős.Ha a vizsgálandó minta valós idejű fluoreszcens RT-PCR amplifikációs eredménye pozitív, az bizonyítja, hogy a SARS-CoV-2 jelen van a mintában.Lásd P2.
A SARS-CoV-2 nukleinsav-meghatározás P2 lépései (valós idejű fluoreszcens RT-PCR)
A SARS-CoV-2 nukleinsav kimutatására vonatkozó laboratóriumi feltételek és követelmények
A nukleinsav-tesztelő laboratóriumok a legideálisabbak a negatív nyomású környezetben, és oda kell figyelniük a nyomás ellenőrzésére, a levegő áramlásának fenntartására és az aeroszolok kiküszöbölésére.A nukleinsav-tesztelő személyzetnek megfelelő képesítéssel kell rendelkeznie, megfelelő polimeráz láncreakciós képzésben kell részesülnie, és át kell mennie az értékelésen.A laboratóriumot szigorúan kell kezelni, zónázni kell, és irreleváns személyeknek szigorúan tilos belépniük.A tiszta területet szellőztetni és fertőtleníteni kell.A megfelelő tárgyakat zónákban helyezik el, a tiszta és koszos tárgyakat elkülönítik, időben kicserélik, és a helyükön fertőtlenítik.Rutinfertőtlenítés: Nagyobb területeken a klórtartalmú fertőtlenítő a fő megoldás, kis területeken pedig 75%-os alkohol használható.Az aeroszolok kezelésének jó módja az ablakok kinyitása a szellőzés érdekében, és a levegő fertőtlenítése ultraibolya sugarakkal, szűréssel és légfertőtlenítéssel is elvégezhető.
A SARS-CoV-2 nukleinsav-meghatározás kulcsfontosságú kapcsolatai és paraméterei (valós idejű fluoreszcens RT-PCR)
Bár a laboratóriumok általában nagy figyelmet fordítanak a nukleinsav „kimutatására”, valójában a nukleinsav „kivonása” is a sikeres kimutatás egyik kulcsfontosságú lépése, amely szorosan összefügg a vírusminták gyűjtésével és tárolásával.
Jelenleg a legelterjedtebb légúti minták, így a nasopharyngealis tamponok a második módszert alkalmazzák, amely egy nukleinsav extrakción és lízisoldaton alapuló inaktiváló (konzerváló) oldat.Egyrészt ez a víruskonzerváló oldat denaturálhatja a vírus fehérjét, elveszíti aktivitását és már nem fertőző, valamint javítja a szállítási és kimutatási szakasz biztonságát;másrészt közvetlenül képes feltörni a vírust, hogy felszabadítsa a nukleinsavat, eltávolítsa a nukleinsavbontó enzimet, és megakadályozza a vírust.Az RNS lebomlik.
Nukleinsav extrakciós lízisoldat alapján készített vírusminta-oldat.A fő komponensek a kiegyensúlyozott sók, etilén-diamin-tetraecetsav kelátképző szer, guanidinsó (guanidin-izotiocianát, guanidin-hidroklorid stb.), anionos felületaktív anyag (dodekán) nátrium-szulfát, kationos felületaktív anyag (tetradecil-trimetil-ammónium-oxalát, p-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-,-tetraecetsav-tetraecetsav. egyéb több vagy több komponens.Jelenleg sokféle nukleinsav extrakciós készlet létezik, és különböző nukleinsav extrakciós és tisztító reagenseket használnak.Még ha ugyanazt a nukleinsav extrakciós és tisztító reagenst használjuk is, az egyes készletek extrakciós eljárásai eltérőek.
Jelenleg a National Medical Products Administration által jóváhagyott nukleinsav-detektáló kit termékeket a SARS-CoV-2 genomban található ORF1ab, E és N gének alapján választják ki.A különböző termékek kimutatási elve alapvetően megegyezik, de a primerek és a szondák kialakítása eltérő.Léteznek egycélú szegmensek (ORF1ab), kettős célszegmensek (ORF1ab, N vagy E) és három célszegmensek (ORF1ab, N és E).A detektálás és az értelmezés, a nukleinsav-kivonás és a valós idejű fluoreszcens RT-PCR reakciórendszer közötti különbséget a vonatkozó kit utasításokban kell figyelembe venni, és ajánlott, hogy a felhasználók szigorúan kövessék a kit értelmezési útmutatójában meghatározott értelmezési módszert.A valós idejű fluoreszcens RT-PCR-rel amplifikált közös régiókat, primereket és próbaszekvenciákat a P3 mutatja.
P3 A SARS-CoV-2 amplikon célpontjának elhelyezkedése a genomon, valamint a primerek és próbák szekvenciája
A SARS-CoV-2 nukleinsav-meghatározás eredményeinek értelmezése (Real-Time fluoreszcens RT-PCR)
„A SARS-CoV-2 fertőzés pneumónia megelőzési és ellenőrzési terve (második kiadás)” először tisztázta az egyetlen génamplifikáció eredményeinek megítélésének kritériumait:
1. Nincs Ct vagy Ct≥40 negatív;
2. Ct<37 pozitív;
3. A 37-40 közötti Ct érték a szürkeárnyalatos terület.A kísérlet megismétlése javasolt.Ha a Ct<40 ismételt eredmény és az amplifikációs görbe nyilvánvaló csúcsokat mutat, a mintát pozitívnak ítélik meg, ellenkező esetben negatívnak.
Az útmutató harmadik kiadása és az útmutató negyedik kiadása folytatta a fenti kritériumokat.A kereskedelmi készletekben használt különböző célpontok miatt azonban az útmutató fent említett 3. kiadása nem adta meg a célpontok kombinációjának meghatározásának kritériumait, hangsúlyozva, hogy a gyártó által megadott utasítások az irányadóak.Az iránymutatások ötödik kiadásától kezdve két célt pontosítottak, különösen az egyetlen, nehezen megítélhető cél megítélési kritériumait.Ez azt jelenti, hogy ha a laboratórium meg akarja erősíteni, hogy egy eset pozitív SARS-CoV-2 nukleinsav kimutatására, akkor a következő 2 feltétel közül egynek teljesülnie kell:
(1) A SARS-CoV-2 két célpontja (ORF1ab, N) ugyanabban a mintában valós idejű fluoreszcens RT-PCR-rel pozitívnak bizonyult.Ha egyetlen cél pozitív, újbóli mintavételre és újbóli vizsgálatra van szükség.Ha a teszt eredménye Ha az egyetlen célpont továbbra is pozitív, akkor pozitívnak minősül.
(2) A valós idejű fluoreszcens RT-PCR két mintája egyidejűleg egyetlen célpontot mutatott pozitívnak, vagy két azonos típusú minta egyetlen célpozitív teszteredményt mutatott, amely pozitívnak tekinthető.Az irányelvek ugyanakkor azt is hangsúlyozzák, hogy a nukleinsav-teszt negatív eredményei nem zárhatják ki a SARS-CoV-2 fertőzést.Ki kell zárni az álnegatív eredményt okozó tényezőket, ideértve a rossz mintaminőséget (légúti minták a szájgaratból és más részekből), a túl korai vagy túl késői mintavételt, a mintákat nem tárolták, szállították és dolgozták fel megfelelően, és magában a technológiában is voltak problémák (vírusvariáció, PCR gátlás) stb.
Hamis negatívok okai a SARS-CoV-2 kimutatásban
A jelenleg szóban forgó „álnegatív” nukleinsav-teszt fogalma gyakran „álnegatív”-ra utal, amelyekben a nukleinsav-teszt eredményei nincsenek összhangban a klinikai megnyilvánulásokkal, azaz a klinikai tünetek és a képalkotó eredmények erősen gyanúsak a COVID-19-re, de a nukleinsavtesztek sokszor mindig „negatívak”.Az Országos Egészségügyi Bizottság Klinikai Laboratóriumi Központja elmagyarázta a „fals negatív” SARS-CoV-2 tesztet.
(1) A fertőzött személy sejtjeiben bizonyos mennyiségű vírus található.A meglévő adatok azt mutatják, hogy a szervezet vírusfertőzése után a vírus az orron és a szájon keresztül a torkába, majd a légcsőbe és a hörgőkbe jut, majd az alveolusokba jut.A fertőzött személy átéli a lappangási időszakot, enyhe tüneteket, majd a súlyos tünetek folyamatát, és a betegség különböző szakaszait.És a vírus mennyisége a test különböző részein eltérő.
A sejttípusok vírusterhelését tekintve alveoláris hámsejtek (alsó légutak)> légúti hámsejtek (felső légutak)> fibroblasztok, endoteliális sejtek és makrofágok stb.;a minta típusából alveoláris mosófolyadék (a legkiválóbb)>mélyköhögő köpet>orrgarat tampon>oropharyngeális tampon>vér.Ezenkívül a vírus a székletben is kimutatható.A kezelés kényelmét és a betegek befogadhatóságát figyelembe véve azonban az általánosan alkalmazott klinikai mintarendelés a szájgarat tampon>orrgarat tampon> hörgő mosófolyadék (összetett műtét) és mély köpet (általában száraz köhögés, nehezen elérhető).
Emiatt egyes betegek oropharynx vagy nasopharynx sejtjeiben a vírus mennyisége kicsi vagy rendkívül alacsony.Ha csak az oropharynxból vagy a nasopharynxből vesznek mintát vizsgálat céljából, a vírus nukleinsavat nem mutatják ki.
(2) A mintagyűjtés során nem gyűjtöttek vírust tartalmazó sejteket, vagy a vírusnukleinsavat nem őrizték meg hatékonyan.
[① Nem megfelelő gyűjtési hely, például oropharyngealis tamponok vételekor a begyűjtési mélység nem elegendő, az összegyűjtött nasopharyngealis tamponokat nem gyűjtik az orrüreg mélyén stb. A begyűjtött sejtek többsége vírusmentes sejt lehet;
② A mintavételi tamponokat helytelenül használják.A tamponfej anyagaként például szintetikus szálakat, például PE-szálat, poliészterszálat és polipropilénszálat ajánlunk.A tényleges működés során természetes szálakat, például pamutot használnak (erős fehérje adszorpciója és nem könnyű kimosni) és nylonszálakat (rossz vízfelvétel, ami elégtelen mintamennyiséghez vezet);
③A vírustároló csövek helytelen használata, például a polipropilén vagy polietilén műanyag tárolócsövek helytelen használata, amelyek könnyen felszívják a nukleinsavakat (DNS/RNS), ami a nukleinsav koncentrációjának csökkenését eredményezi a tárolóoldatban.A gyakorlatban polietilén-propilén polimer műanyag és néhány speciálisan kezelt polipropilén műanyag tartály használata javasolt a vírusos nukleinsavak tárolására.]
[① Nem megfelelő gyűjtési hely, például oropharyngealis tamponok vételekor a begyűjtési mélység nem elegendő, az összegyűjtött nasopharyngealis tamponokat nem gyűjtik az orrüreg mélyén stb. A begyűjtött sejtek többsége vírusmentes sejt lehet;
② A mintavételi tamponokat helytelenül használják.A tamponfej anyagaként például szintetikus szálakat, például PE-szálat, poliészterszálat és polipropilénszálat ajánlunk.A tényleges működés során természetes szálakat, például pamutot használnak (erős fehérje adszorpciója és nem könnyű kimosni) és nylonszálakat (rossz vízfelvétel, ami elégtelen mintamennyiséghez vezet);
③A vírustároló csövek helytelen használata, például a polipropilén vagy polietilén műanyag tárolócsövek helytelen használata, amelyek könnyen felszívják a nukleinsavakat (DNS/RNS), ami a nukleinsav koncentrációjának csökkenését eredményezi a tárolóoldatban.A gyakorlatban polietilén-propilén polimer műanyag és néhány speciálisan kezelt polipropilén műanyag tartály használata javasolt a vírusos nukleinsavak tárolására.]
(4) A klinikai laboratóriumi működés nem szabványosított.A minta szállítási és tárolási körülményei, a klinikai laboratóriumok szabványosított működése, az eredmények értelmezése és minőségellenőrzése a kulcstényezők a vizsgálati eredmények pontosságának és megbízhatóságának biztosításához.Az Országos Egészségügyi Bizottság Klinikai Laboratóriumi Központja által 2020. március 16-24-én végzett külső minőségértékelés eredménye szerint az érvényes eredményt kapott 844 laboratórium közül 701 (83,1%) minősített, 143 (16,9%) nem.Minősített, az általános laboratóriumi vizsgálati feltételek jók, de a különböző laboratóriumokban továbbra is eltérések mutatkoznak a személyzet működési képességében, az egyetlen célpont pozitív mintaértelmezési képességében és a minőségellenőrzésben.
Hogyan csökkenthető a SARS-CoV-2 nukleinsav kimutatásának álnegatív száma?
Az álnegatívok csökkentését a nukleinsav-detektálásban a hamis negatívok előállításának négy szempontja alapján kell optimalizálni.
(1) A fertőzött személy sejtjeiben bizonyos mennyiségű vírus található.A vírus koncentrációja a feltételezett fertőzöttek testének különböző részein különböző időpontokban eltérő lesz.Ha nincs garat, akkor hörgőmosó folyadékban vagy székletben lehet.Ha több típusú mintát lehet gyűjteni egy időben vagy a betegség előrehaladásának különböző szakaszaiban vizsgálat céljából, segít elkerülni a hamis negatív eredményeket.
(2) A mintagyűjtés során vírust tartalmazó sejteket kell gyűjteni.Ez a probléma a mintagyűjtők képzésének erősítésével nagymértékben megoldható.
(3) Megbízható IVD-reagensek.A reagensek kimutatási teljesítményértékelésének országos szintű kutatásával, a fennálló problémák megvitatásával tovább javítható a reagensek detektálási hatékonysága, javítható az elemzés érzékenysége.
(4) A klinikai laboratóriumok szabványosított működése.A laboratóriumi személyzet képzésének erősítésével, a laboratóriumi minőségirányítási rendszer folyamatos fejlesztésével, az ésszerű felosztások biztosításával, a személyzet észlelési képességének javításával csökkenthető a nem megfelelő laboratóriumi működésből adódó téves negatívok száma.
A SARS-CoV-2 nukleinsav teszt újbóli pozitív eredményének okai felépült és hazabocsátott betegeknél
A „COVID-19 diagnosztikai és kezelési terv (Trial Seventh Edition)” egyértelműen előírja, hogy a COVID-19-betegek gyógyulásának és a kórházból való hazabocsátásának egyik kritériuma az, hogy két egymást követő légúti minta nukleinsav-tesztje negatív legyen (legalább 24 órás különbséggel), de nagyon kevés oka van annak, hogy a SARS-CoV-2 nukleáris tesztje ismét pozitív volt a savban.
(1) A SARS-CoV-2 egy új vírus.Tovább kell ismerni a kórokozó mechanizmusát, az okozott betegség teljes képét és a betegség lefolyásának jellemzőit.Ezért egyrészt meg kell erősíteni az elbocsátott betegek kezelését és 14 napos orvosi megfigyelést kell végezni.Nyomon követés, egészségügyi monitorozás és egészségügyi útmutatás végrehajtása a betegség előfordulásának, kialakulásának és kimenetelének teljes folyamatának megértése érdekében.
(2) Előfordulhat, hogy a beteg újra megfertőződött a vírussal.Zhong Nanshan akadémikus azt mondta: Mivel a gyógyult betegekben antitestek vannak, a SARS-CoV-2 antitestekkel eltávolítható, amikor ismét megtámadják.Sok oka lehet, ami lehet a gyógyult beteg oka, vagy összefügghet a vírus mutációjával, esetleg laboratóriumi vizsgálattal.Ha maga a vírus, akkor a SARS-CoV-2 mutáció miatt a felépült beteg által termelt antitest hatástalanná válhat a mutáns vírussal szemben.Ha a beteg ismét megfertőződik a mutált vírussal, a nukleinsav teszt ismét pozitív lehet.
(3) Ami a laboratóriumi vizsgálati módszereket illeti, minden vizsgálati módszernek megvannak a maga korlátai.A SARS-CoV-2 nukleinsav kimutatása a génszekvencia megválasztásának, a reagensek összetételének, a módszer érzékenységének és egyéb okoknak köszönhető, ami ahhoz vezet, hogy a meglévő kiteknek saját alsó kimutatási határaik vannak.A beteg kezelését követően a vírus a szervezetben csökken.Ha a vizsgálandó mintában a vírusterhelés az alsó kimutatási határ alatt van, „negatív” eredmény jelenik meg.Ez az eredmény azonban nem jelenti azt, hogy a vírus teljesen eltűnt a szervezetben.A vírus a kezelés leállítása után jelentkezhet.Resurgence”, folytassa a másolást.Ezért ajánlatos hetente egyszer felülvizsgálni az elbocsátást követő 2-4 héten belül.
(4) A nukleinsav a vírus genetikai anyaga.A vírus elpusztul, miután a beteg vírusellenes kezelésen esett át, de a fennmaradó vírus RNS-fragmensek továbbra is megmaradnak az emberi szervezetben, és nem ürülnek ki teljesen a szervezetből.Néha, bizonyos körülmények között, jobban megtartható.Hosszú ideig, és ekkor a nukleinsav teszt „átmenetileg” pozitív lesz.A beteg felépülési idejének meghosszabbodásával, miután a szervezetben lévő maradék RNS fragmentumok fokozatosan kimerülnek, a nukleinsav teszt eredménye negatívra fordulhat.
(5) A SARS-CoV-2 nukleinsav-teszt eredménye csak a vírus RNS jelenlétét vagy hiányát bizonyítja, és nem tudja igazolni a vírus aktivitását és azt, hogy a vírus átvihető-e.Bizonyítani kell, hogy az ismét pozitív nukleinsavteszttel rendelkező beteg újra fertőzésforrássá válik-e.A klinikai mintákon vírustenyésztést kell végezni, és „élő” vírust kell tenyészteni annak bizonyítására, hogy fertőző.
Összegzés
Összefoglalva, a SARS-CoV-2 nukleinsav teszt hamis negatív, újrateszt pozitív eredményét és más olyan állapotokat, amelyek nincsenek összhangban a klinikai megnyilvánulásokkal, nem lehet teljesen elkerülni.A tényleges szűrésben és tesztelésben javasolt a klinikai tünetek, képalkotó vizsgálatok (CT) és kísérletek kombinálása A laboratóriumi vizsgálat (nukleinsav-teszt + vírusspecifikus antitest-vizsgálat) eredményeit az átfogó diagnózis érdekében, hogy elkerülhető legyen a diagnózis elmulasztása és a téves diagnózis.Ha a vizsgálati eredmények nyilvánvalóan ellentmondanak a klinikai megnyilvánulásoknak, ajánlatos a teljes vizsgálati kapcsolat átfogó elemzését elvégezni (mintagyűjtés, keringési és feldolgozási kapcsolatok), hogy kizárják a SARS-CoV-2 vírus korai fertőzését, ismétlődő fertőzését vagy más légúti vírusfertőzéssel kombinált fertőzéseket stb.Ha a körülmények megengedik, ajánlatos érzékenyebb mintákat, például köpetet vagy alveoláris mosófolyadékot gyűjteni újbóli vizsgálat céljából.
Kapcsolódó termékek:
SARS-CoV-2 nukleinsav-detektáló készlet (multiplex PCR fluoreszcens szonda módszer)
Feladás időpontja: 2021.03.03