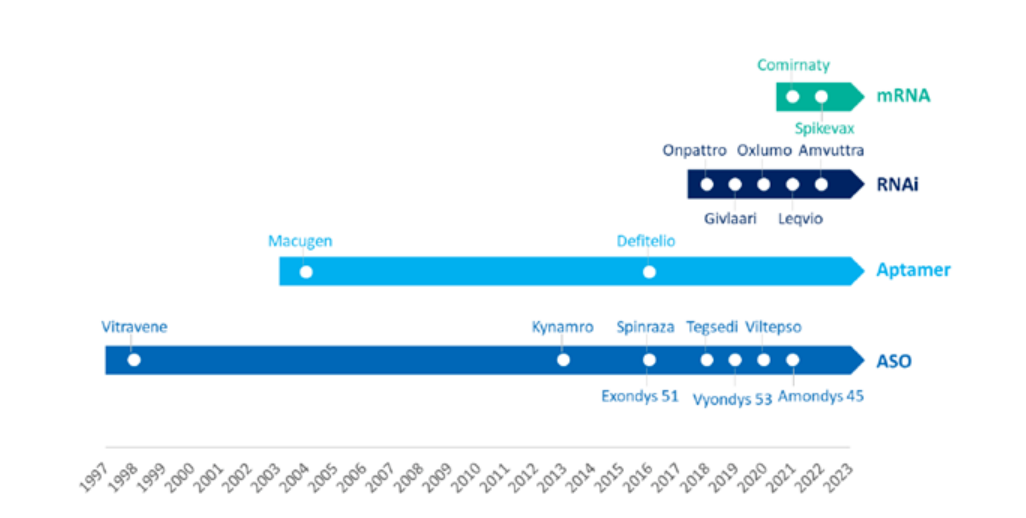
Forrás: WuXi AppTec
Az elmúlt években az RNS-terápia területe robbanásszerű tendenciát mutatott.Csak az elmúlt 5 évben 11 RNS-terápiát hagyott jóvá az FDA, és ez a szám még a korábban jóváhagyott RNS-terápiák összegét is meghaladja!A hagyományos terápiákhoz képest az RNS-terápia gyorsan kifejleszthet célzott terápiákat, amelyek sikeresebbek, mindaddig, amíg a célpont génszekvenciája ismert.Másrészt a legtöbb RNS-terápia továbbra is csak ritka betegségek kezelésére áll rendelkezésre, és az ilyen terápiák fejlesztése továbbra is számos kihívással néz szembe a terápia tartóssága, biztonsága és szállítása tekintetében.A mai cikkben aA WuXi AppTec tartalomcsapata áttekinti az RNS-terápia területén az elmúlt évben elért előrehaladást, és olvasóival együtt várja ennek a feltörekvő területnek a jövőjét.
▲ 11 RNS-terápiát vagy vakcinát hagyott jóvá az FDA az elmúlt 5 évben
A ritka betegségektől a gyakori betegségekig több virág nyílik
Az új koronajárványban a semmiből született meg az mRNS-oltás, amely széleskörű figyelmet kapott az ipar részéről.Azutánáttörést jelent a fertőző betegségek elleni vakcinák fejlesztésében, az mRNS-technológia másik nagy kihívása az alkalmazási kör kiterjesztése több betegség kezelésére és megelőzésére.
Közöttük,Az egyénre szabott rákvakcinák az mRNS technológia fontos alkalmazási területei, és több rák elleni védőoltás pozitív klinikai eredményét is láthattuk ebben az évben.Éppen ebben a hónapban jelent meg a Moderna és a Merck által közösen kifejlesztett, egyénre szabott rákvakcina a Keytruda PD-1 gátlóval kombinálva.csökkentette a kockázatotstádiumú melanoma III. és IV. stádiumban szenvedő betegeknél a teljes tumorreszekció után 44%-kal csökkent (a Keytruda monoterápiához képest).A sajtóközlemény rámutatott, hogy ez az első alkalom, hogy egy mRNS rák elleni vakcina hatékonyságot mutatott be a melanoma kezelésében egy randomizált klinikai vizsgálat során, ami mérföldkőnek számít az mRNS rák elleni vakcinák kifejlesztésében.
Ezenkívül az mRNS-vakcinák a sejtterápia terápiás hatását is fokozhatják.Például a BioNTech egy tanulmánya rámutatott arra, hogy ha a betegeket először alacsony dózisú CLDN6-célzott CAR-T terápiával adják be.BNT211, majd CLDN6-ot kódoló mRNS vakcinával injektálva in vivo stimulálhatják a CAR-T sejteket azáltal, hogy CLDN6-ot expresszálnak az antigénprezentáló sejtek felszínén.Erősítés, ezáltal fokozza a rákellenes hatást.Az előzetes eredmények azt mutatták, hogy a kombinált terápiában részesülő 5 betegből 4, azaz 80% ért el részleges választ.
A betegségek körének bővítésében az mRNS terápia mellett az oligonukleotid terápia és az RNSi terápia is jó eredményeket ért el.A krónikus hepatitis B kezelésében a betegek közel 30%-a nem képes in vivo kimutatni a hepatitis B felületi antigént és a hepatitis B vírus DNS-ét az antiszensz oligonukleotid terápia után.a GSK és az Ionis által közösen kifejlesztett bepirovirsen24 hétig.Egyes betegeknél még 24 héttel a kezelés leállítása után is ezek a hepatitis B markerek még mindig nem voltak kimutathatók a szervezetben.
Véletlenül az RNSi terápiaA Vir Biotechnology és az Alnylam által közösen kifejlesztett VIR-2218-at egyesítettékα-interferonnal, és a 2. fázisú klinikai vizsgálatok során a krónikus hepatitis B-betegek körülbelül 30%-ánál sem sikerült kimutatni a hepatitis B felszíni antigént (HBsAg).Ezenkívül ezeknél a betegeknél antitestek alakultak ki a hepatitis B fehérje ellen, ami pozitív immunrendszeri választ mutatott.Ezeket az eredményeket összesítve az iparág rámutat arra, hogy az RNS-terápia lehet a kulcsa a hepatitis B funkcionális gyógyításának.
Ez csak a kezdete lehet a gyakori betegségek RNS-terápiájának.Az Alnylam kutatás-fejlesztési folyamata szerint magas vérnyomás, Alzheimer-kór és nem alkoholos steatohepatitis kezelésére is fejleszt RNSi-terápiákat, és érdemes előre tekinteni a jövőre.
Áttörni az RNS-terápia szűk keresztmetszetét
Az RNS-terápia alkalmazása az egyik szűk keresztmetszet, amely korlátozza alkalmazását.A tudósok számos olyan technológiát is fejlesztenek, amelyek specifikusan RNS-terápiát juttatnak el a májon kívüli szervekhez és szövetekhez.
Az egyik lehetséges módszer a terápiás RNS-ek „megkötése” szövetspecifikus molekulákkal.Például az Avidity Biosciences nemrégiben bejelentette, hogy technológiai platformja képes monoklonális antitesteket kapcsolni oligonukleotidokhoz.hatékonyan kötik az siRNS-eket.vázizomba küldik.A sajtóközlemény rámutatott, hogy ez az első alkalom, hogy az siRNS-t sikeresen meg lehet célozni és emberi izomszövetbe juttatni, ami jelentős áttörést jelent az RNS-terápia területén.
A kép forrása: 123RF
Az antitestkonjugációs technológia mellett számos lipid nanorészecskéket (LNP) fejlesztő cég is „frissíti” az ilyen hordozókat.Például, ReCode Therapeuticegyedülálló Selective Organ Targeting LNP Technology (SORT) segítségével különféle típusú RNS-terápiát juttat a tüdőbe, lépbe, májba és más szervekbe.Idén a cég bejelentette, hogy lezárult egy 200 millió dolláros B sorozatú finanszírozási kör, amelyben a Pfizer, a Bayer, az Amgen, a Sanofi és más nagy gyógyszergyártó cégek kockázati tőke részlege vesz részt a beruházásban.A Kernal Biologics, amely idén szintén 25 millió dolláros A-sorozat finanszírozásban részesült, olyan LNP-ket is fejleszt, amelyek nem halmozódnak fel a májban, de mRNS-t képesek eljuttatni a célsejtekhez, például az agyhoz vagy bizonyos daganatokhoz.
Az idén debütált Orbital Therapeutics szintén kulcsfontosságú fejlesztési iránynak tekinti az RNS-terápia átadását.Az RNS-technológia és a szállítási mechanizmusok integrálásával a vállalat egy olyan egyedülálló RNS-technológiai platform kiépítését várja, amely meghosszabbítja az innovatív RNS-terápiák perzisztenciáját és felezési idejét, és eljuttatja azokat különféle sejt- és szövettípusokhoz.
A történelmi pillanatban az RNS-terápia új típusa jelenik meg
Idén december 21-ig az RNS-terápia területén 31 korai fázisú finanszírozási esemény történt (részletesen lásd a módszertant a cikk végén), 30 élvonalbeli cég bevonásával (egy cég kétszer kapott finanszírozást), összesen 1,74 milliárd dollár finanszírozási összeggel.Ezeknek a cégeknek az elemzése azt mutatja, hogy a befektetők optimistábbak azokkal az élvonalbeli vállalatokkal kapcsolatban, amelyektől az RNS-terápia számos kihívásának megoldását várják, annak érdekében, hogy teljes mértékben kiaknázzák az RNS-terápiában rejlő lehetőségeket, és több beteg számára előnyösek legyenek.
És vannak feltörekvő cégek, amelyek teljesen új típusú RNS-terápiákat fejlesztenek ki.A hagyományos oligonukleotidoktól, RNSi-től vagy mRNS-től eltérően az e cégek által kifejlesztett új típusú RNS-molekulák várhatóan áttörik a meglévő terápiák szűk keresztmetszetét.
A cirkuláris RNS az egyik legforróbb pont az iparban.A lineáris mRNS-hez képest az Orna Therapeutics nevű élvonalbeli cég által kifejlesztett cirkuláris RNS technológia elkerülheti, hogy a veleszületett immunrendszer és az exonukleázok felismerjék, ami nemcsak jelentősen csökkenti az immunogenitást, hanem nagyobb stabilitást is biztosít.Ezenkívül a lineáris RNS-hez képest a cirkuláris RNS felhajtott konformációja kisebb, és több cirkuláris RNS is betölthető ugyanazzal az LNP-vel, javítva az RNS-terápia szállítási hatékonyságát.Ezek a tulajdonságok segíthetnek javítani az RNS-terápiák hatékonyságát és tartósságát.
Ebben az évben a cég egy 221 millió dolláros B sorozatú finanszírozási kört zárt le, valamint elért egy kutatási ésfejlesztési együttműködés a Merck-kel 3,5 milliárd USD-ig.Ezenkívül az Orna cirkuláris RNS-t is használ a CAR-T terápia közvetlen előállítására állatokban, ezzel bizonyítvakoncepció.
A cirkuláris RNS mellett az önerősítő mRNS (samRNAs) technológiát is kedvelték a befektetők.Ez a technológia az RNS-vírusok önamplifikációs mechanizmusán alapul, amely képes a samRNS-szekvenciák replikációját indukálni a citoplazmában, meghosszabbítva az mRNS-terápiák expressziós kinetikáját, ezáltal csökkentve a beadás gyakoriságát.A hagyományos lineáris mRNS-hez képest a samRNS képes fenntartani hasonló fehérje expressziós szintet körülbelül 10-szer alacsonyabb dózisban.Ebben az évben az RNAimmune, amely ennek a területnek a fejlesztésére összpontosít, 27 millió amerikai dollárt kapott az A sorozatból.
A tRNS technológiát is érdemes várni.A tRNS-alapú terápia „figyelmen kívül hagyhatja” a rossz stopkodont, amikor a sejt fehérjét állít elő, így a normál, teljes hosszúságú fehérje termelődik.Mivel sokkal kevesebb típusú stopkodon létezik, mint a kapcsolódó betegségek, a tRNS-terápia képes egyetlen terápia kifejlesztésére, amely számos betegség kezelésére alkalmas.Ebben az évben a hC Bioscience, amely a tRNS-terápiára összpontosít, összesen 40 millió USD-t gyűjtött össze az A sorozatú finanszírozásból.
Epilógus
Feltörekvő kezelési modellként az RNS-terápia gyors fejlődést ért el az elmúlt években, és számos terápiát jóváhagytak.Az iparág legújabb fejlesztéseiből látható, hogy az élvonalbeli RNS-terápiák kiterjesztik az ilyen terápiákkal kezelhető betegségek körét, leküzdik a célzott bejuttatás különböző szűk keresztmetszeteit, és új RNS-molekulákat fejlesztenek ki, hogy leküzdjék a meglévő terápiák hatékonysági és tartóssági korlátait.több kihívás.Az RNS-terápia ezen új korszakában ezek az élvonalbeli vállalatok az iparág középpontjába kerülhetnek a következő néhány évben.
Kapcsolódó termékek:
https://www.foreivd.com/cell-direct-rt-qpcr-kit-taqman-product/
https://www.foreivd.com/cell-direct-rt-qpcr-kit-direct-rt-qpcr-series/
Feladás időpontja: 2022. december 27